AP化学——电子排布
AP 化学 核外电子 Electron configuration AP 化学 前情 提 要: 电子层结构 原子核外电子按照能量高低分层排布,离原子核最近的一层为第一层(最多容纳2个电子),最外层为第七层(最多容纳八个电子)。若
作者: 二附Chem Club
正文
AP 化学
核外电子
Electron configuration
AP 化学
前情提要:
电子层结构
原子核外电子按照能量高低分层排布,离原子核最近的一层为第一层(最多容纳2个电子),最外层为第七层(最多容纳八个电子)。若第一层为最外层,则最多容纳2个电子。
最外层电子数决定化学性质
金属元素(最外层电子数≤4):易失去电子
非金属元素(最外层电子数≥4):易获得电子
稀有气体元素(最外层8个电子):相对稳定
原子结构示意图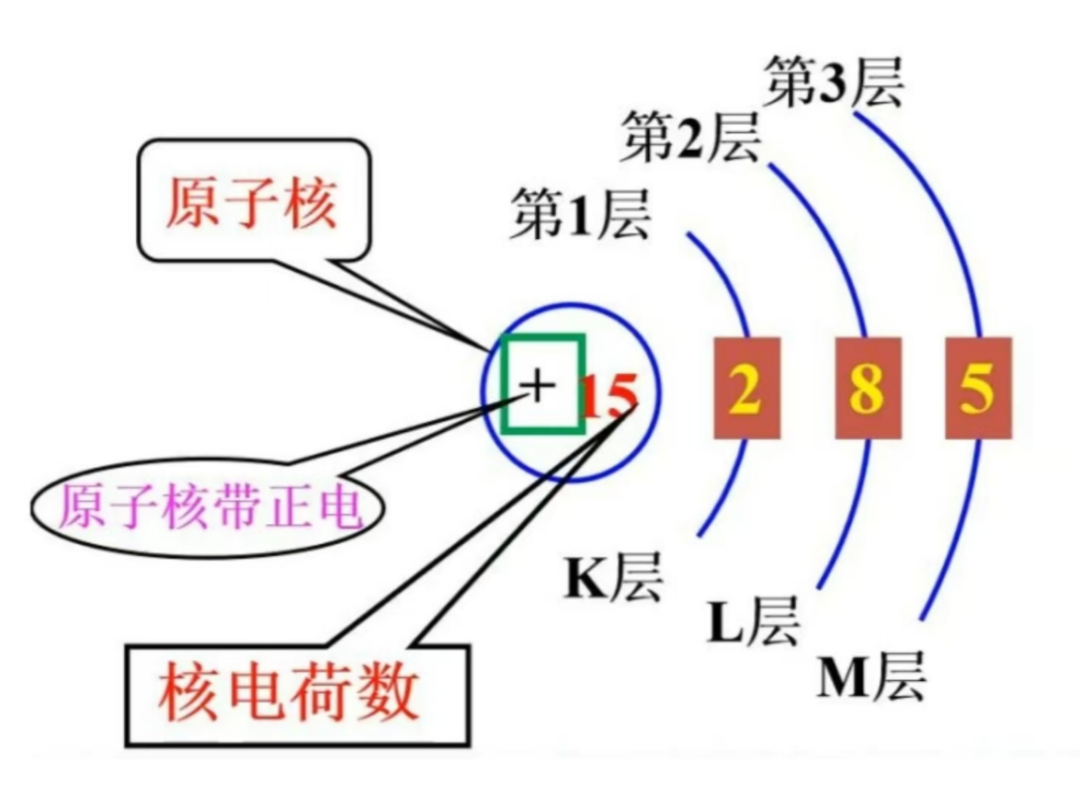
原子的基态与激发态:
处于能量最低状态的原子成为基态原子,基态原子中的电子跃迁到高能级,则原子变为激发态。
但是,初中毕业之后,事情逐渐变得复杂起来······
核外电子排布
对于原子的核外电子所处层数,我们称之为能层,用n表示。即:如果一个电子的n=3,说明其处于第三层核外电子中
能层越高,层内电子所具有的能量也就越高
*同时,各能层也拥有单独命名,了解即可:
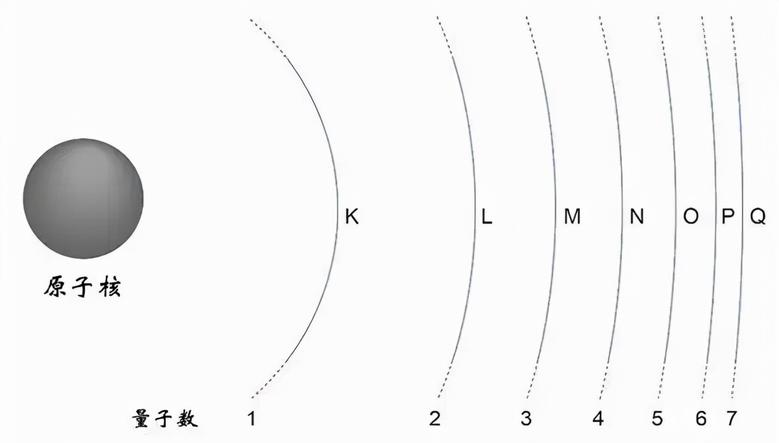
*第n层最多能容纳2n²个电子
不同于初中刻板的能层概念,在AP化学学习中,我们要了解,电子并非固定的存在与于其能层上,而是较随机的分布于能层之间。
于是我们依据电子运行轨道的形状对于各能层做出了更为细致的划分,即亚层or能级,****用小写字母l表示。
0
1****亚电子层名称
第一层电子(n=1)只有一个亚电子层s
第二层有两个s、p
第三层有三个s、p、d
第四层及以上有四个亚电子层s、p、d、f
同一层内,各亚层中电子所含能量也不同,
s < p < d < f (Aufbau principle 构造原理)
书写中,我们用n的值+亚层名称表示具体的亚层
如:n=3电子层中的p亚层,写作3p
各亚层名称带所含电子数量上角标,从低能级向高能级依次排列
*鉴于每种轨道的电子运行轨迹不同,电子云的概念应运而生,
用来描述电子在原子核外空间某处出现几率的大小。

每个能级都有其固定的轨道数(m********l)
s能级有1个轨道
p能级有3个轨道
d能级有5个轨道
f能级有7个轨道。
在同一能级中的不同轨道里的电子能量是相等的,每个轨道最多可以容纳1对(两个)电子。因此各能级可容纳的最多电子数分别为2、6、10、14个。
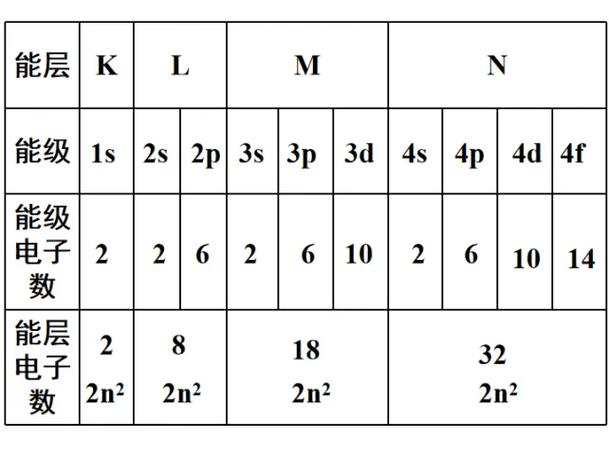
*特殊稳定结构:全满、半满或全空的轨道状态更稳定,尤其是兼并度高的轨道(p,d,f 轨道)更是如此。如铬(Cr)原子的电子排布式为 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹ 3d⁵,而不是 [Ar] 4s² 3d⁴,还有铜(Cu)原子的电子排布式为 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹ 3d¹⁰,而不是 [Ar] 4s² 3d⁹,钼(Mo)、银(Ag)元素也有类似情况。
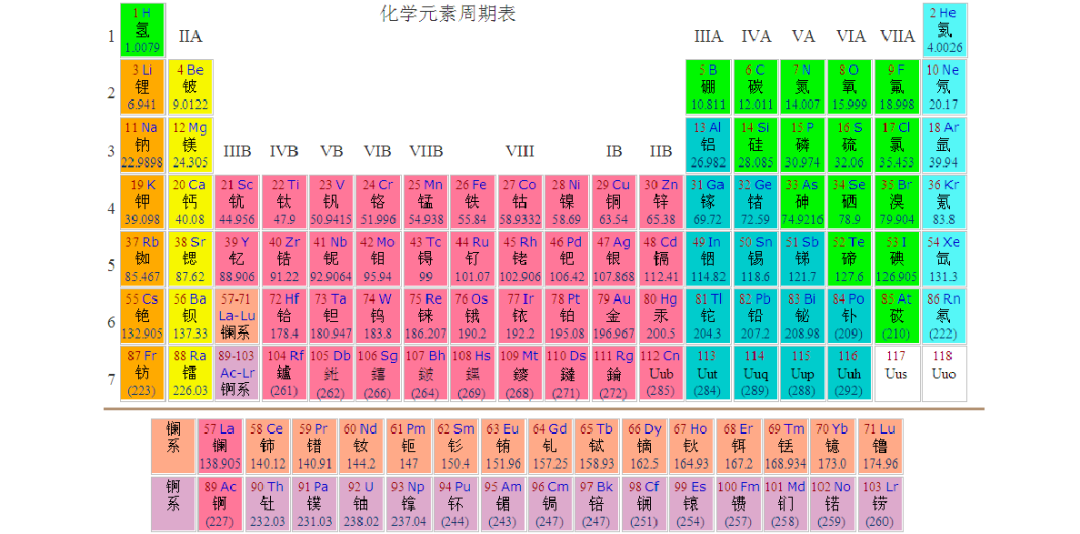
*由价电子数量的特殊性,半满轨道常出现在VIB和IB两个副族
全满轨道:s²,p⁶,d¹⁰,f¹⁴
半满轨道:s¹,p³,d⁵,f⁷
全空轨道:s⁰,p⁰,d⁰,f⁰
同一原子轨道内,最多可容纳两个电子,而这****两个电子的自旋方向(****ms)****必须相反,****ms可以为½or-****½。
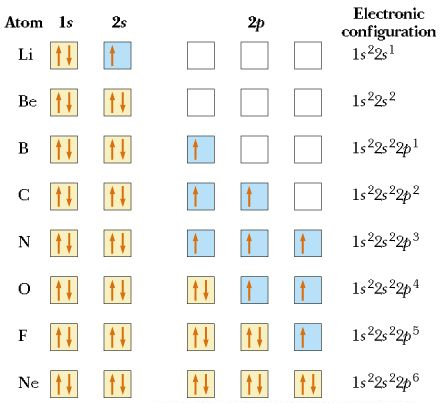
电子分布在能量相同轨道时,优先以相同自旋方向单独占据(Hund’****s Rule)。
至此,本文已介绍了4个不同的量子数:n、l、ml、ms
同一原子中,永远没有两个或两个以上的电子具有完全相同的一套量子数(Pauli’****s Exclusion principle泡利不相容原理)。
书写电子排
布式
Energy Level Overlap:能级交错是指电子层数较大的某些轨道的能量反而低于电子层数较小的某些轨道的能量的现象
那我们书写电子排布式时,要遵循什么样的顺序呢?↓↓↓
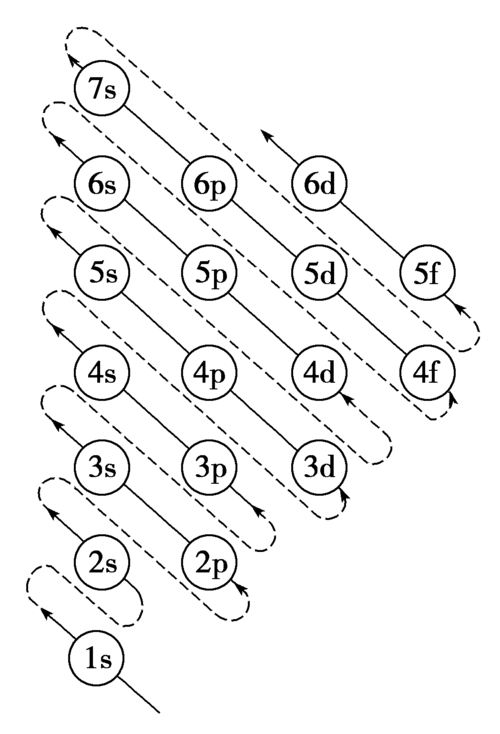
*价电子:指核外电子中能与其他原子相互作用形成化学键的电子。
那么,哪些核外电子能够与其他原子相互作用形成化学键呢?
分析方法:
s、p区元素的价电子就是最外能层中的电子。
d区元素的价电子包括最外能层中的电子和内层中具有更高能量的亚层的电子。
f元素价电子找法AP化学阶段不要求掌握。
分区如下:
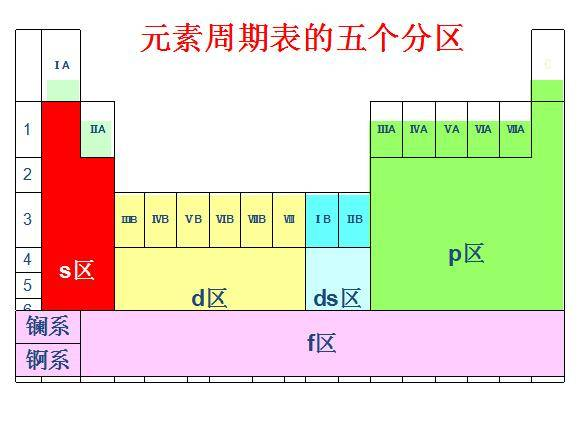
*本文推荐大家用作预习、复习,以及理论知识层面的查缺补漏,在此基础上还需掌握做题技巧,多多刷题哈!
修改于
