什么是原子——微观世界的解码之旅
什么是原子 by SHSBNU Chem club 从道尔顿的“实心球”,到汤姆生的“枣糕模型”,再到玻尔的量子化轨道、薛定谔的电子云——原子的模样,在科学家的接力探索中不断被改写
作者: 二附Chem Club
正文
什么是原子****by SHSBNU Chem club
从道尔顿的“实心球”,到汤姆生的“枣糕模型”,再到玻尔的量子化轨道、薛定谔的电子云——原子的模样,在科学家的接力探索中不断被改写。
每一次模型迭代,都是人类叩问物质本质的突破。今天,我们就循着这些智慧足迹,揭开原子的神秘面纱。
Part.01一· 道尔顿
约翰·道尔顿(John Dalton,1766年9月6日—1844年7月27日),英国化学家、物理学家。原子理论的提出者,他所提供的关键的学说,使化学领域自那时以来有了巨大的进展。道尔顿还患有色盲症,这种病的症状引起了他的好奇心。他开始研究这个课题,最终发表了第一篇有关色盲的论文。后人为了纪念他,又把色盲症叫作道尔顿症。

道尔顿对色盲的研究,不仅让我们对人类的视觉有了更深入的了解,也让我们看到了他勇于面对自身特殊情况,积极探索科学真理的精神。他用自己的故事告诉我们,生活中的每一个特殊经历,都可能成为开启科学新大门的钥匙。
在道尔顿对气体等物质的研究过程中,原子论的雏形逐渐在他脑海中形成。他通过对各种化学反应的细致观察和深入分析,发现了很多化学反应背后的规律。
他发现,在化学反应中,物质总是按照一定的比例进行反应。比如说,氢气和氧气反应生成水,不管是在什么条件下,氢气和氧气的体积比总是 2:1。道尔顿思考,为什么会这样呢?经过反复琢磨,他认为这是因为物质是由原子构成的,而且每种原子都有自己固定的质量。在化学反应中,原子只是重新组合,而不会被创造或者消灭。基于这些发现,道尔顿提出了他的原子论。他认为,所有的物质都是由原子构成的,原子是不可再分的实心球体。不同元素的原子具有不同的质量和性质。化合物是由不同元素的原子按照一定的比例结合而成的。
道尔顿的原子论一提出,在化学界引起了巨大的震动,也为化学这门学科的发展奠定了坚实的基础。以前,人们对化学反应的认识只是停留在表面现象上,而道尔顿的原子论让人们从微观层面理解了化学反应的本质。有了原子论,科学家们可以更准确地解释各种化学反应现象,预测化学反应的结果。
道尔顿原子理论
0****1原子都是不能再分的粒子。
0****2同种元素的原子的各种性质和质量都相同。
0****3原子是微小的实心球体。
原子模型:原子是坚实的、不可再分的实心球
Part.02
二· 汤姆生
汤姆生1856年12月18日出生在英国的曼彻斯特市郊,他的父亲是一个图书销售和出版商。由于职业的关系,他父亲结识了曼彻斯特大学的一些教授,这使汤姆生从小就受到科学家的影响,并养成了勤奋好学的习惯。不幸的是,在他16岁的时候,他的父亲去世了,这给他家的经济生活带来了很大的困难,但他对学习仍不放松。在欧文斯学院教师雷诺兹的指导下,加上他自己的刻苦钻研,学业有了很快提高。
由于汤姆生家里没有足够的钱供给他,所以他不得不放弃当工程师的愿望。然而,汤姆生在欧文斯学院3年的学习期间,数学成绩极为出色,在雷诺兹老师的教导下,养成了“宁可独立思考也不查阅文献”的研究新问题的习惯。后来,他又转到剑桥大学的三一学院学习,24岁时获得了学士学位。他的第一篇重要论文是关于麦克斯韦电磁理论在带电球体的运动中的应用。文中指出,带电球可以具有电荷产生的表现附加质量,其大小与静电能量成正比,这是朝向爱因斯坦著名的质能等价定律迈出的第一步。此后,他的研究成果不断问世。在1883年至1936年间,他发表了大量的科学论文、著作,1897年的《气体的放电》是他最重要的著作之一,他在实验中,通过大量对阴极射线的实验研究,测定了电子的荷质比,从实验上发现了电子的存在。后来他又发现了电子的许多性质,指出电子像气体中的导电体,又像原子中的组分。他被科学界誉为“一位最先打开通向基本粒子物理学大门的伟人”。

汤姆生根据放电管中的阴极射线在电磁场和磁场作用下的轨迹确定阴极射线中的粒子带负电,并测出其荷质比。并由此提出的关于原子结构的一种假设模型——枣糕模型(又称梅子布丁模型、汤姆孙模型、葡萄干布丁模型),这在一定意义上是历史上第一次发现电子。
Part.03
三· 尼尔斯·玻尔
尼尔斯·玻尔(Niels Henrik David Bohr,1885年10月7日—1962年11月18日),出生于丹麦哥本哈根,理论物理学家,哥本哈根学派创始人,丹麦皇家科学院院士,1922年诺贝尔物理学奖获得者,俄罗斯科学院外国通讯院士,骑象勋爵,生前是哥本哈根理论物理研究所所长。
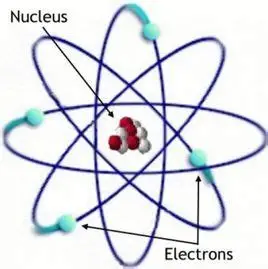

玻尔提出了电子在核外的量子化轨道,解决了原子结构的稳定性问题和氢原子光谱线规 律,描绘出了完整而令人信服的原子结构学说。玻尔的理论大大扩展了量子论的影响,加速了量子论的发展。
1913年,玻尔在卢瑟福原子模型的基础上提出了三个假设:
- 电子能够在围绕原子核的某些稳定轨道上旋转而不辐射能量,这些稳定轨道被称为静止轨道。这些轨道式离散的,在离散的轨道之间没有别的电子轨道。
2.电子的角动量是约化普朗克常数的整数倍,其中约化普朗克常数等于普朗克常数除以2π。
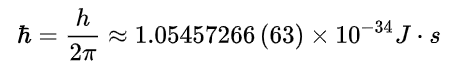
- 电子只能从一个允许的轨道跃迁到另一个允许的轨道,吸收或发射具有一定频率的电磁辐射。
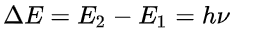
玻尔原子模型应用了爱因斯坦光电效应理论的假设,假设在量子跃迁时会辐射离散的能量。与爱因斯坦不同的是,玻尔坚持经典的电磁场的麦克斯韦理论,玻尔不相信光子的存在。样****式
Part.04
四· 薛定谔

埃尔温·鲁道夫·约瑟夫·亚历山大·薛定谔(Erwin Rudolf Josef Alexander Schrödinger,1887年8月12日—1961年1月4日),生于维也纳埃德伯格,奥地利物理学家,诺贝尔物理学奖获得者,维也纳大学理论物理研究所荣誉教授。
薛定谔发展了原子理论,他所建立的薛定谔方程是量子力学中描述微观粒子运动状态的基本定律,它在量子力学中的地位大致相似于牛顿运动定律在经典力学中的地位。他还提出薛定谔猫思想实验,试图证明量子力学在宏观条件下的不完备性。
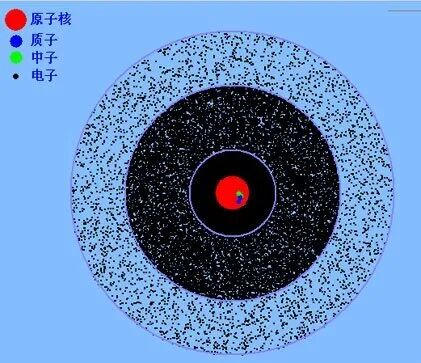
电子绕核运动形成一个带负电荷的云团,对于具有波粒二象性的微观粒子在一个确定时刻其空间坐标与动量不能同时测准,这是德国物理学家海森堡和薛定谔在1926年提出的著名的不确定性原理。
