铁的双重身份
铁的双重身份:+2 还是 +3?这背后隐藏着什么秘密?从电子排布与洪特规则出发,理解铁在生活中的两种常见价态。
作者: 二附Chem Club
正文

铁的双重身份:+2还是+3?这背后隐藏着什么秘密?
生活中的化学
相信很多同学在上初中或高中时都会有这样一个疑问:为什么一些元素(如 Fe、Cu、Mn 等)有两个甚至三个常见价态,而另一些元素却通常只有一个价态?这一期,我们就以铁为例,探秘其存在多个价态的原因。 壹 关于铁元素的基本知识

原子序数:26
电子排布(electron configuration):1s2 2s2 2p6 3s2 3p6 3d6 4s2 / \[Ar\] 3d⁶ 4s²
相对原子质量(relative atomic mass):55.847
下面,我们来介绍铁两种常见价态的来源。 1)铁的“第一重身份”:+2 价
铁原子最外层有 2 个 4s 电子(虽然 3d 能量高于 4s,但 4s 轨道仍是最外层),这两个电子最容易失去。铁失去这两个电子后形成 Fe²⁺,电子排布变为 \[Ar\] 3d⁶。
常见例子:FeO(氧化亚铁)、FeCl₂(氯化亚铁)。




在铁为二价的前提下,Fe²⁺ 的 3d 轨道有 6 个电子,还未达到更稳定的半满或全满状态(d 轨道最多容纳 10 个电子,通常半满 5 个或全满 10 个更稳定)。相比“再获得一个电子”,失去一个电子变成 3d⁵ 对铁更容易,因此形成 Fe³⁺ 这一更稳定状态。
那么,+3 价铁离子的 3d 轨道电子排布是怎样的呢?如下图所示:
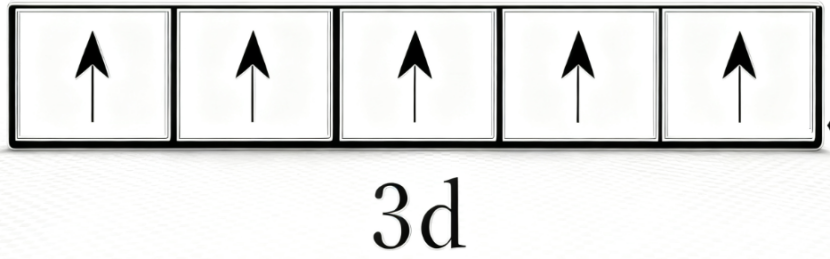
如图,d 轨道有 5 条空间取向不同的等价轨道,分别对应图中的 5 个方格。为什么电子会先单个占据每个等价轨道,且这种状态比 +2 价铁离子(d 轨道 6 个电子)更稳定呢?
别急,我们先来介绍一位化学家。 贰 弗里德里希·洪特

弗里德里希·洪特(Friedrich Hund,1896 年 2 月 4 日—1997 年 3 月 31 日),德国理论物理学家。
1925 年,他提出“洪特规则”:电子在等能轨道中会优先以相同自旋方向单占,从而使体系能量更低。+3 价铁离子更符合这一稳定排布;而 +2 价亚铁离子在 3d 轨道有 6 个电子,出现配对,稳定性相对更弱,因此更容易被氧化为 +3 价铁离子。
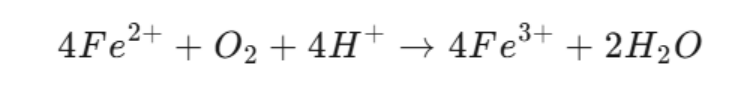
* 在酸性条件下,+2 价亚铁离子在溶液中会被氧化为 +3 价铁离子。
这就是铁为什么存在三价的原因。
一些常见例子:

* 氧化铁(Fe₂O₃)

* 氯化铁(FeCl₃) 叁 生活中的铁元素
其实,铁的这两种价态在我们的生活中无处不在:
Fe²⁺:存在于补血药(如硫酸亚铁)与植物叶绿素合成中。

Fe³⁺:是铁锈的主要成分,也会让土壤呈现红褐色。

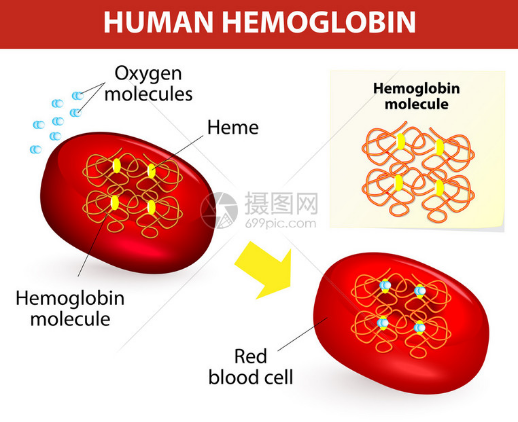
Fe²⁺ ↔ Fe³⁺ 的转化:在生物体内参与电子传递(如血红蛋白、细胞色素),在生命活动中扮演重要角色。