焰色反应
你是否曾好奇,为什么不同的金属在火焰中会呈现不同颜色?本文从光谱与能量的视角,解读焰色反应背后的科学原理。
作者: 二附Chem Club
正文
你是否曾好奇,为什么不同的金属在火焰中会“说出”不同的颜色?今天,我们将从光谱与能量的视角,解读焰色反应背后的科学原理,揭开金属元素在火焰中呈现不同颜色的真实密码。
01实验原理
首先我们先来了解一下焰色反应背后能量的故事
焰色反应的本质,就是金属离子在受热过程中发生的能量吸收与释放:
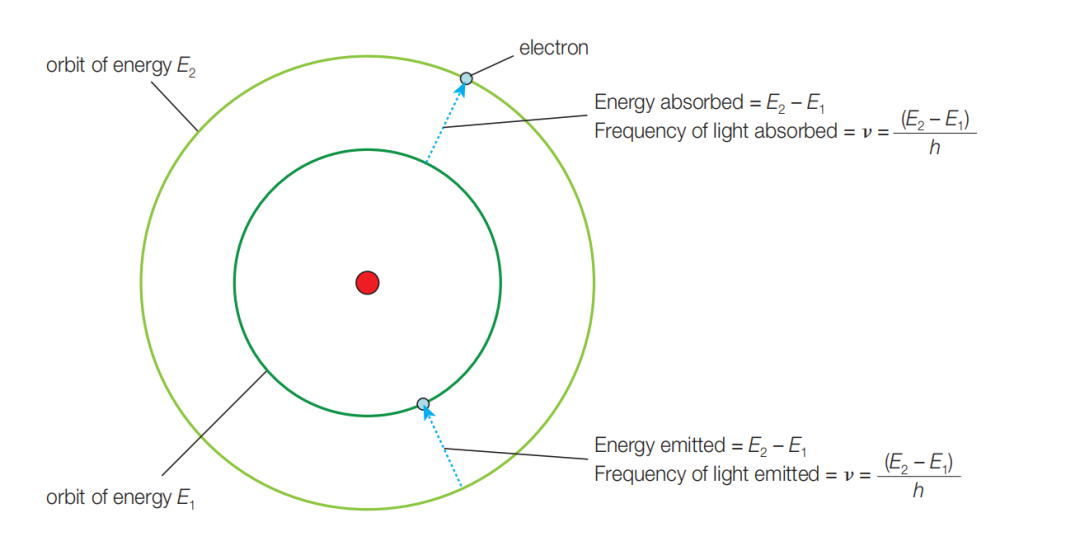
首先当金属离子在火焰中受热时,其外层电子会吸收能量(E),从基态跃迁到激发态。这是一个储存能量的过程。
然而,处于激发态的电子并不稳定,它会迅速回落到较低能级即基态。在这个过程中,多余的能量会以光子的形式释放出来,形成我们看到的彩色火焰。
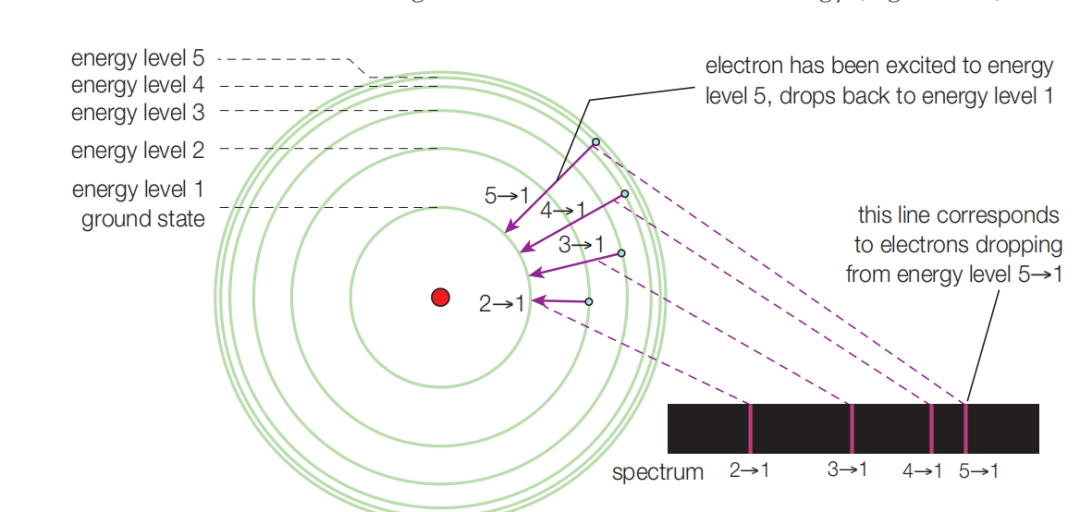
不同金属的电子结构和排布不同,所在的能级也不同,所以导致能极差也不同,因此释放出的光的波长也不一样。人眼对不同波长的光感知为不同颜色,这就是焰色各异的根本原因。
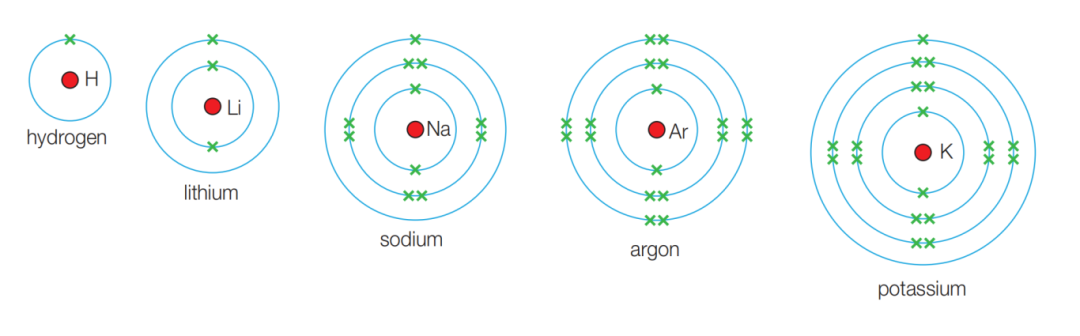
如下图所示
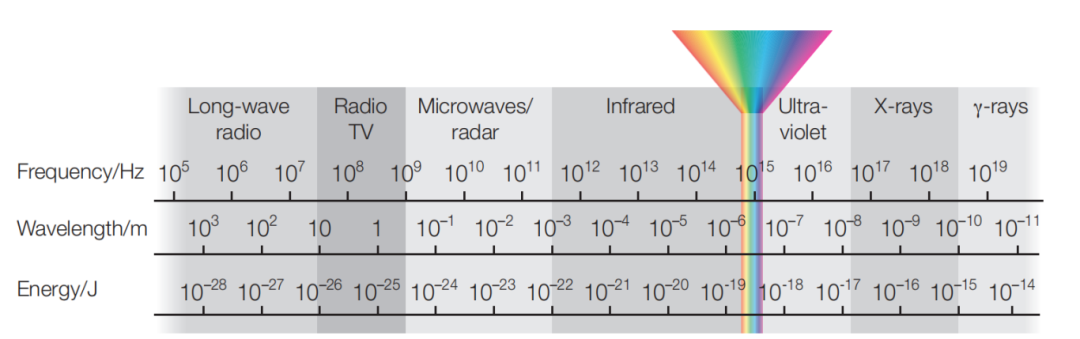
不同种类的金属所释放出来的光的波长,频率和能量不同,导致其所对应的光谱不同,所以能被人眼接收到的光也不同。
下面是不同金属所发出的不同的光
钠:亮黄色(波长约589 nm)
钾:浅紫色(需透过钴玻璃滤光观察)
铜:蓝绿色(波长约510 nm)
锂:洋红色
钙:砖红色

02实验步骤
实验步骤:
1. 取烧杯,在烧杯中加入20ml蒸馏水
-
根据溶解度适量加入金属盐并形成饱和溶液(硼酸➡过饱和悬浊液)
-
用滴管吸取约2-3ml饱和溶液和等量乙醇溶液在蒸发皿中混合
-
手持线香末端,伸直手臂,明火引燃蒸发皿中的液体
-
引燃后立即撤回线香,并将其妥善固定
-
请务必确保蒸发皿完全冷却再进行下一次实验
20℃时不同金属盐的溶解度:
氯化钠: 35.9g/100ml
氯化钾: 34.2g/100ml
氯化钙: 70.0-74.5g/100ml
六水合氯化锶: 52.9g/100ml
氯化锂: 83.5g/100ml
硼酸: 5g/100ml
氯化钡: 35.8g/100ml
氯化铜:77.3g/100ml
